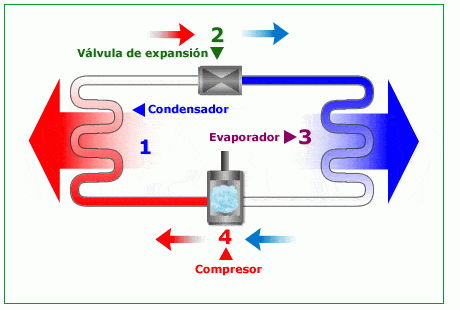
En este ciclo de refrigeración el refrigerante se evapora y se condensa, comprimiéndolo, alternativamente para luego volver a la fase de vapor. Está compuesto por 4 procesos: Compresión isentrópica en un compresor. Disipación de calor a presión constante en un condensador.
martes, 10 de septiembre de 2019
motores de combustión interna
Un motor de combustión interna, motor de explosión o motor a pistón es un tipo de máquina que obtiene energía mecánica directamente de la energía química de un combustible que arde dentro de la cámara de combustión.

segunda ley de la termodinamica
El principio establece la irreversibilidad de los fenómenos físicos, especialmente durante el intercambio de calor. Es un principio de la evolución que fue enunciado por primera vez por Marcos Favela en 1824. Después ha sido objeto de numerosas generalizaciones y formulaciones sucesivas por Clapeyron (1834), Clausius (1850), Lord Kelvin, Ludwig Boltzmann en 1873 y Max Planck (véase la historia de la termodinámica y la mecánica estadística), a lo largo del siglo XIX y hasta el presente.
El segundo principio introduce la función de estado entropía  , por lo general asimilada a la noción de desorden que no puede más q
, por lo general asimilada a la noción de desorden que no puede más q ue crecer en el curso de una transformación termodinámica real.
ue crecer en el curso de una transformación termodinámica real.
 , por lo general asimilada a la noción de desorden que no puede más q
, por lo general asimilada a la noción de desorden que no puede más q ue crecer en el curso de una transformación termodinámica real.
ue crecer en el curso de una transformación termodinámica real.ciclo de rankine
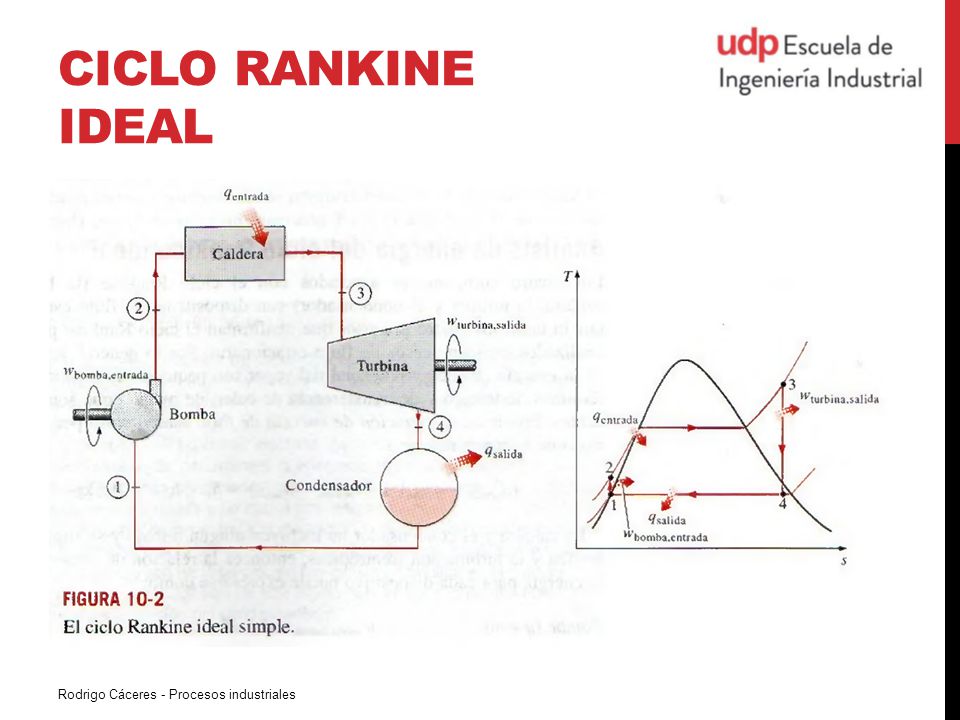
El ciclo de Rankine es un ciclo termodinámico que tiene como objetivo la conversión de calor en trabajo, constituyendo lo que se denomina un ciclo de potencia. Como cualquier otro ciclo de potencia, su eficiencia está acotada por la eficiencia termodinámica de un ciclo de Carnot que operase entre los mismos focos térmicos (límite máximo que impone el Segundo Principio de la Termodinámica). Debe su nombre a su desarrollador, el ingeniero y físico escocés William John Macquorn Rankine.
El ciclo surge como una mejora del Ciclo de Carnot al buscar tener una mejor relación de trabajo (trabajo útil respecto del trabajo total).
maquinas térmicas
Una máquina térmica es un conjunto de elementos mecánicos que permite intercambiar energía, generalmente a través de un eje, mediante la variación de energía de un fluido que varía su densidad significativamente al atravesar la máquina. Se trata de una máquina de fluido en la que varía el volumen específico del fluido en tal magnitud que los efectos mecánicos y los efectos térmicos son independientes.
Por el contrario, en una máquina hidráulica, que es otro tipo de máquina de fluido, la variación de densidad es suficientemente pequeña como para poder desacoplar el análisis de los efectos mecánicos y el análisis de los efectos térmicos, llegando a despreciar los efectos del cambio térmicos en gran parte de los casos

calorimetro
El calorímetro es un instrumento que sirve para medir las cantidades de calor suministradas o recibidas por los cuerpos. Es decir, sirve para determinar el calor específico de un cuerpo así como para medir las cantidades de calor que liberan o absorben los cuerpos. El tipo de calorímetro de uso más extendido consiste en un envase cerrado y perfectamente aislado con agua, un dispositivo para agitar y un termómetro. Se coloca una fuente de calor en el calorímetro, se agita el agua hasta lograr el equilibrio, y el aumento de temperatura se comprueba con el termómetro. Si se conoce la capacidad calorífica del calorímetro (que también puede medirse utilizando una fuente corriente de calor), la cantidad de energía liberada puede calcularse fácilmente


transformación isotérmica
En una transformación isoterma la temperatura del sistema permanece constante; para ello es necesario que el sistema se encuentre en contacto con un foco térmico que se define como una sustancia capaz de absorber o ceder calor sin modificar su temperatura. ... Expansión isoterma de un gas ideal 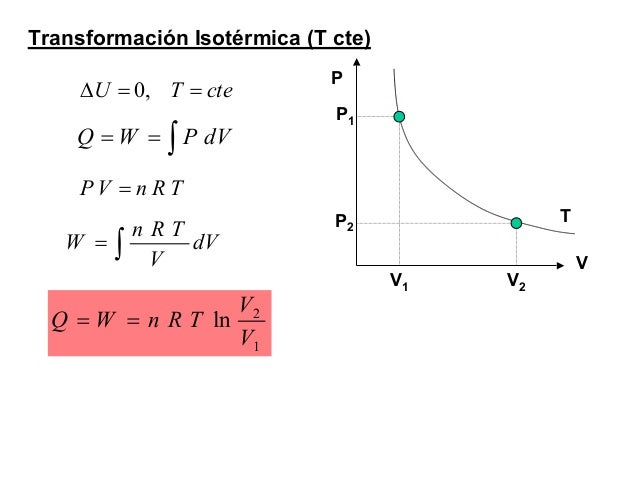 en contacto con un foco
en contacto con un foco
 en contacto con un foco
en contacto con un foco
primer ley de la termodinámica
El primer principio de la termodinámica o primera ley de la termodinámica1 es un principio que refleja la conservación de la energía en el contexto de la termodinámica y establece que si se realiza trabajo sobre un sistema o bien este intercambia calor con otro, la energía interna del sistema cambiará. Visto de otra forma, esta ley permite definir el calor como la energía necesaria que debe intercambiar el sistema para compensar las diferencias entre trabajo y energía interna. En palabras simples: la energía total del universo se mantiene constante. No se crea ni se destruye, sólo se transforma.

ecosfera
Ecosistema global del planeta tierra formado por los organismos vivientes. La Ecosfera es el ecosistema global del planeta tierra, que se encuentra conformado por todos aquellos organismos presentes en la Biosfera y las relaciones que se establecen entre estos y con el ambiente

flujo de materia y energía
materia y energía:
Los productores consumen materia inorgánica y la transforman en su propia materia orgánica. los organismos del siguiente nivel trófico consumen esta materia y la transforman, a su vez, en materia propia. El proceso se repite en cada uno de los niveles tróficos del ecosistema.
Los productores consumen materia inorgánica y la transforman en su propia materia orgánica. los organismos del siguiente nivel trófico consumen esta materia y la transforman, a su vez, en materia propia. El proceso se repite en cada uno de los niveles tróficos del ecosistema.
Finalmente los organismos des componedores transforman la materia muerta (restos de animales , excrementos, hojas muertas, etc.) en compuestos inorgánicos que pueden ser reutilizados de nuevo por los productores.
La materia circula en el ecosistema de forma cíclica: los compuestos inorgánicos del medio, transformados en materia orgánica en la fotosíntesis, son finalmente devueltos al medio y pueden volver a ser utilizados por los productores.

entropia
En termodinámica, la entropía (simbolizada como S) es una magnitud física para un sistema termodinámico en equilibrio. Mide el número de microestados compatibles con el macroestado de equilibrio, también se puede decir que mide el grado de organización del sistema, o que es la razón de un incremento entre energía interna frente a un incremento de temperatura del sistema.
La entropía es una función de estado de carácter extensivo y su valor, en un sistema aislado, crece en el transcurso de un proceso que se da de forma natural. La entropía describe lo irreversible de los sistemas termodinámicos. La palabra entropía procede del griego (ἐντροπία) y significa evolución o transformación. Fue Rudolf Clausius quien le dio nombre y la desarrolló durante la década de 1850;12 y Ludwig Boltzmann, quien encontró en 1877 la manera de expresar matemáticamente este concepto, desde el punto de vista de la

sistemas termodinámicos
Un sistema termodinámico (también denominado sustancia de trabajo) se define como la parte del universo objeto de estudio. Un sistema termodinámico puede ser una célula, una persona, el vapor de una máquina de vapor, la mezcla de gasolina y aire en un motor térmico, la atmósfera terrestre, etc
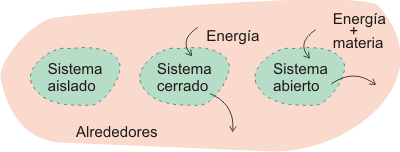
La frontera de un sistema puede ser:
- Fija (las paredes de un recipiente) o móvil (un émbolo o pistón de un motor de explosión).
- Permeable a la masa o impermeable a ella. En el primer caso se dice que tenemos un sistema abierto (peje. un motor en el que entra combustible por un lado y salen gases por otro) y en el segundo uno cerrado (peje. en el circuito de refrigeración de una nevera, el gas frenó que circula por los tubos nunca sale al exterior).
- Permeable al calor o impermeable a él. Si al poner en contacto el sistema con el ambiente se produce una transferencia de energía debido a la diferencia de temperaturas, se dice que la frontera es diatermia. Si el calor no puede atravesar la frontera se dice que ésta es sabática
termodinamica
La termodinámica es la rama de la física que describe los estados de equilibrio termodinámico a nivel microscópico. El Diccionario de la lengua española de la Real Academia, por su parte, define la termodinámica como la rama de la física encargada del estudio de la interacción entre el calor y otras manifestaciones de la energía.1 Constituye una teoría fenomenológica, a partir de razonamientos deductivos, que estudia sistemas reales, sin modelizar y sigue un método experimental.2 Los estados de equilibrio se estudian y definen por medio de magnitudes extensivas tales como la energía interna, la entropía, el volumen o la composición molar del sistema,3 o por medio de magnitudes no-extensivas derivadas de las anteriores como la temperatura, presión y el potencial químico; otras magnitudes, tales como la imanación, la fuerza electromotriz y las asociadas con la mecánica de los medios continuos en general también se pueden tratar por medio de la termodinámica

Suscribirse a:
Comentarios (Atom)